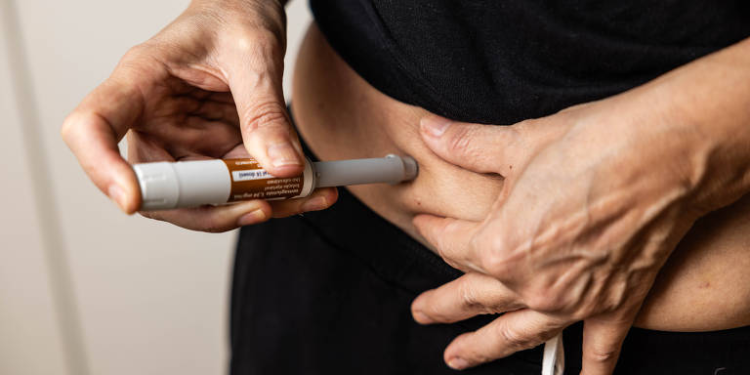
A Agência Nacional de Vigilância Sanitária (Anvisa) emitiu um alerta sobre um risco grave, ainda que raro, relacionado ao uso de medicamentos com semaglutida — substância presente em fármacos populares para emagrecimento como Ozempic®, Wegovy® e Rybelsus®. Segundo a agência, esses remédios podem causar uma reação adversa muito rara chamada neuropatia óptica isquêmica anterior não arterítica (Noiana), que pode levar à perda súbita e irreversível da visão.
A recomendação ocorre após análise do Comitê de Avaliação de Risco em Farmacovigilância (PRAC) da Agência Europeia de Medicamentos (EMA), que identificou a Noiana como um possível evento adverso da semaglutida. No Brasil, o sistema de notificação VigiMed já registrou 52 casos de suspeitas de distúrbios oculares relacionados a essa substância.
Diante do risco, mesmo que raro, a Anvisa determinou que a reação adversa seja incluída nas bulas dos medicamentos com semaglutida. Profissionais da saúde devem alertar seus pacientes sobre os sinais de alerta, como perda repentina ou piora da visão, e orientar sobre a necessidade de interromper imediatamente o tratamento caso os sintomas sejam identificados.
A partir de 23 de junho de 2025, a compra de medicamentos que contêm semaglutida — e outros agonistas GLP-1 — só poderá ser realizada com receita médica retida na farmácia. A medida faz parte da Resolução da Diretoria Colegiada (RDC) nº 973/2025 e da Instrução Normativa (IN) nº 360/2025, ambas publicadas como forma de reforçar a segurança e o controle sobre o uso desses fármacos.
Em nota oficial, a Novo Nordisk, fabricante dos medicamentos citados, afirmou que leva a segurança dos pacientes “muito a sério” e que está em permanente colaboração com autoridades sanitárias para monitorar os riscos. A empresa destacou que os dados obtidos em estudos clínicos — que envolveram mais de 52 mil pacientes — e em avaliações pós-comercialização (equivalentes a mais de 33 milhões de pacientes-ano) não indicam uma relação causal evidente entre a semaglutida e a ocorrência da Noiana.
Mesmo com esse posicionamento, a farmacêutica confirmou que irá colaborar com a EMA e com outros órgãos reguladores para atualizar as bulas dos produtos com a inclusão da nova advertência.
A Anvisa reforça que qualquer evento adverso associado a medicamentos deve ser comunicado por meio do sistema VigiMed, como forma de contribuir para o monitoramento e a segurança do uso desses produtos em todo o país.